应用西格玛度量和稳健算法评价不同检测系统糖化血红蛋白检测结果的可比性
摘要:目的 分析和评价浙江省糖化血红蛋白(HbA1c)项目的检测质量及不同系统检测结果的可比性。方法 收集2018年浙江省HbA1c室间质量评价(EQA)数据,按照检测系统分组。以采用稳健算法计算的5个标本均值为靶值,并计算各组的稳健均值和实验室间的稳健变异系数(CV)。计算每个标本各分组的西格玛水平及加权西格玛水平。结果 将268家实验室中纳入统计分析的实验室按检测系统分为4个组:A组(44家)、B组(87家)、C组(50家)、D组(26家)。5个标本的总体稳健CV依次为2.58%、1.85%、5.05%、2.70%和4.77%。A、B、C、D组的实验室间稳健CV分别为1.80%~3.16%、1.72%~2.64%、1.32%~1.81%、1.67%~3.38%,各组对应的西格玛平均值分别为1.19(-0.35~2.39)、2.42(1.66~3.25)、2.95(2.2~3.44)、0.26(-2.76~2.92)。仅C组有3个标本和B组有1个标本的西格玛水平>3。5个标本的加权西格玛水平分别为2.48、3.00、0.87、2.41和1.30,平均值为2。结论 西格玛度量和稳健统计方法可更深入和客观地分析EQA结果中反馈的HBA1c检测质量水平。浙江省HbA1c检测质量水平尚不理想,需进一步采取质量管理措施,以实现检验结果互认的目标,满足临床诊断糖尿病的需求。
关键词:糖化血红蛋白; 糖尿病; 六西格玛; 室间质量评价; 质量控制;
糖尿病及其慢性并发症已成为全球范围的重大公共卫生问题。我国的糖尿病患者数量位居世界前列,患病率高达9.7%[1-2]。糖化血红蛋白(glycated hemoglobin A1c,HbA1c)可反映既往2~3个月的平均血糖水平,且检测结果的影响因素较少,是评估长期血糖控制状况和疗效观察的重要指标[3]。2010年,美国糖尿病学会(American Diabetes Association,ADA)正式推荐HbA1c为糖尿病的诊断指标之一[4],但我国尚未将HbA1c作为糖尿病诊断标准,也没有中国人群诊断切点,主要原因是我国HbA1c检测方法种类较多,各实验室检测结果的一致性尚不理想[5]。
室间质量评价(e x t e r n a l q u a l i t y assessment,EQA)是临床实验室质量保证的重要方法,通过分析和评价实验室检测中存在的问题,促进实验室检验结果间的可比性,是临床检验结果互认的重要依据。六西格玛可用于检验中过程的性能评价和室内质控规则的设计,还可量化检验前和检验后过程的质量。检验全过程的质量指标结果评价可结合风险管理工具进行,以识别实验室内存在的主要问题[6]。关于西格玛度量用于EQA和检验结果可比性的报道尚不多见,本研究采用稳健统计方法评价HbA1c的EQA结果,并采用西格玛度量评价各检测系统的性能及各系统检测结果的可比性。
1 材料和方法
1.1 质控品
2 0 1 8年浙江省H b A1 c项目EQA中采用5个批号的质控品,分别为20180911(批号为38561)、20180912(批号为38562)、20180913(批号为38542)、20180914(批号为38563)、20180915(批号为38553),均购自美国Bio-Rad公司。
1.2 方法
HbA1c项目的EQA全年共1次,浙江省临床检验中心于2018年4月20日统一将5个标本分发至268家实验室,实验室收到标本后立即检测,并通过Clinet-EQA回报检测结果及使用的检测系统。
2 6 8家实验室均回报了5个标本的检测结果。按照本研究先期介绍的稳健统计算法[7],通过Clinet-EQA软件完成,以各标本的稳健均值作为靶值,以稳健变异系数(coefficient of variation,CV)为总CV。对10家及以上实验室使用的检测系统单独分组,并进一步分析,将使用同一种检测系统的实验室视为一个整体,计算使用同的稳健均值和稳健CV。
采用Microsoft Excel软件,每个分组的偏移(bias,Bias)按照公式:Bias(%)=(组均值-靶值)/靶值×100%计算。以6%允许总误差(allowable total error,TEa)(美国病理学家协会评价标准),按公式:西格玛=(TEa-|Bias|)/CV,计算5个标本各分组的西格玛水平,以评价该检测系统的整体性能。最后结合各分组的实验室数量,计算5个标本的加权西格玛水平。以相同的方式,计算TEa为12%(浙江省临床检验中心EQA评价标准)和7%(国家卫生健康委临床检验中心EQA评价标准)时,5个标本的加权西格玛水平。
1.3 选择室内质控方案
根据计算出的西格玛水平,选择合适的质控方案。以临界系统误差为下横坐标、以西格玛值为上横坐标,以误差检出概率为纵坐标,绘制标准西格玛质控图。曲线表示不同质控规则及检测数的统计效率。见图1。
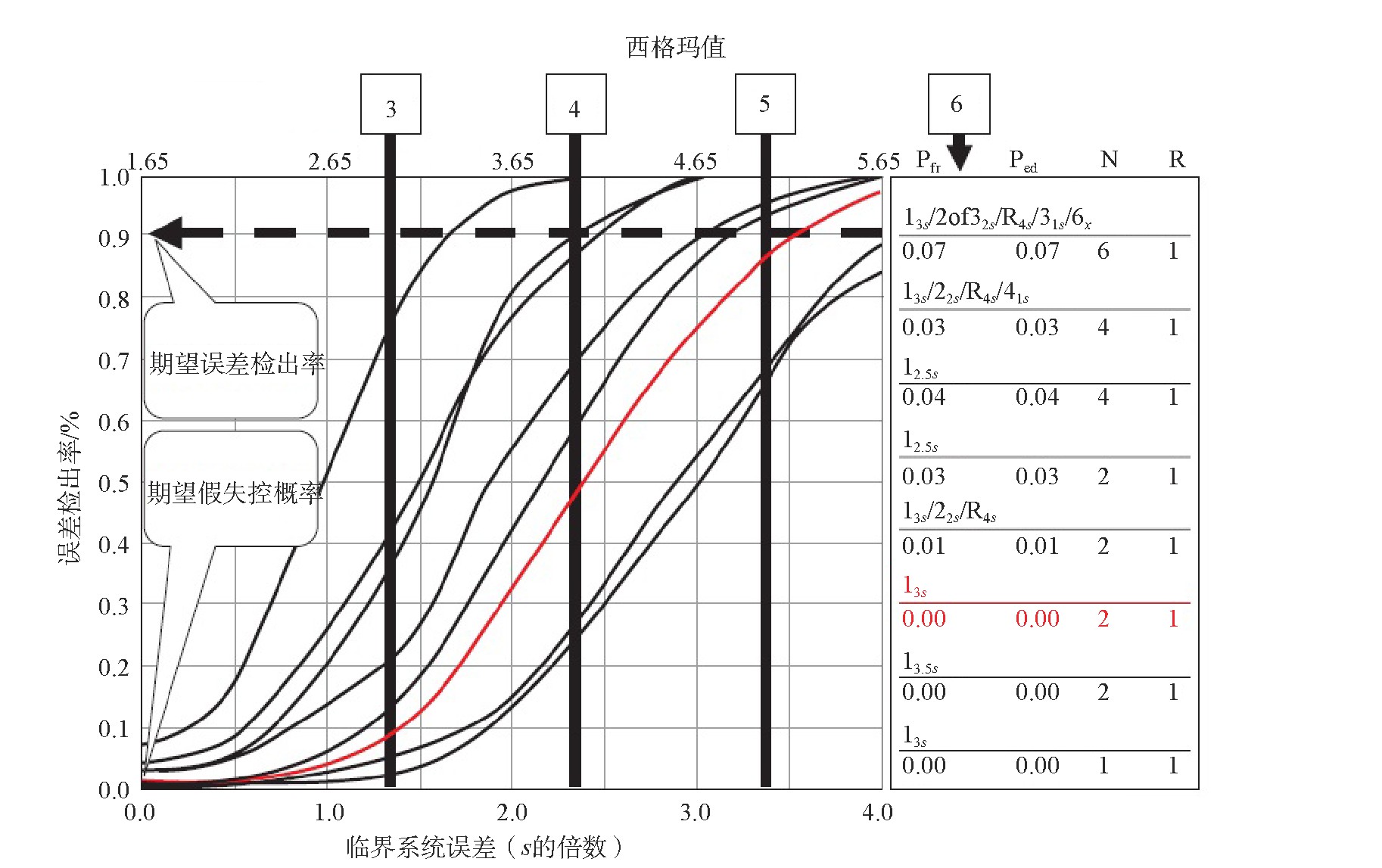 图1 临界系统误差-西格玛质控图
注:Pfr表示假失控概率;Ped表示误差检出概率;R表示分析批次;N表示质控检测数
图1 临界系统误差-西格玛质控图
注:Pfr表示假失控概率;Ped表示误差检出概率;R表示分析批次;N表示质控检测数
2 结果
5个标本的HbA1c检测靶值分别为5.27%、9.53%、9.31%、13.99%和13.49%,对应的CV总分别为2.58%、1.85%、5.05%、2.70%和4.77%。
2.1 不同检测系统的性能特征
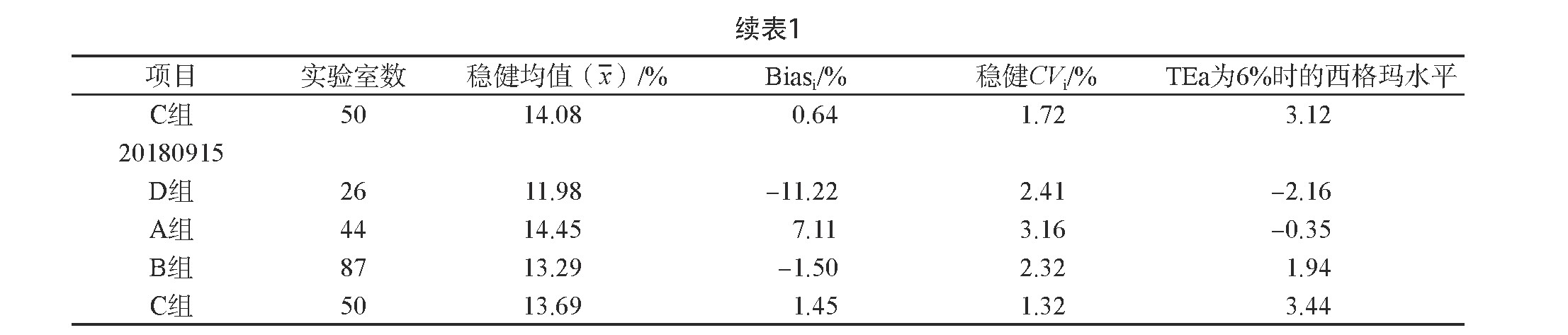
将268家实验室中纳入统计分析的实验室按使用的检测系统分为4个组:A组(44家)、B组(87家)、C组(50家)、D组(26家)。各组的稳健均值、稳健CV及计算得到的Bias见表1。其中C组的实验室间CV较小,5个标本的合成稳健CV为1.68%(1.32%~1.81%);B组、D组、A组5个标本的合成稳健CV分别为2.20%(1.72%~2.64%)、2.43%(1.67%~3.38%)、2.49%(1.80%~3.16%)。C组5个标本的平均Bias最小(1.48%),B组、D组和A组分别为1.76%、2.28%和2.23%。
当TEa为6%时,A组、B组、C组、D组的西格玛平均值分别为1.19(-0.35~2.39)、2.42(1.66~3.25)、2.95(2.20~3.44)、0.26(-2.76~2.92)。仅C组有3个标本和B组有1个标本的西格玛水平>3,其余均<3,甚至为负数。见表1。
表1 各组(不同检测系统)性能特征

2.2 不同质量要求下的西格玛水平
TEa为6%时,5个标本的加权西格玛水平分别为2.48、3.00、0.87、2.41和1.30,平均值为2。TEa为7%和12%时,加权西格玛均值分别为2.50和4.95。见表2。
表2 不同质量要求下的西格玛水平
 2.3 质控方案设计
2.3 质控方案设计
当TEa为6%和7%时,即使选择最严格的质控规则和质控检测数也无法满足误差检出率>90%的目标。当TEa为12%时,可选择单规则12.5s、1批/d和2个检测数/批的质控方案,其误差检出率为95%,假失控概率为3%。见图2。
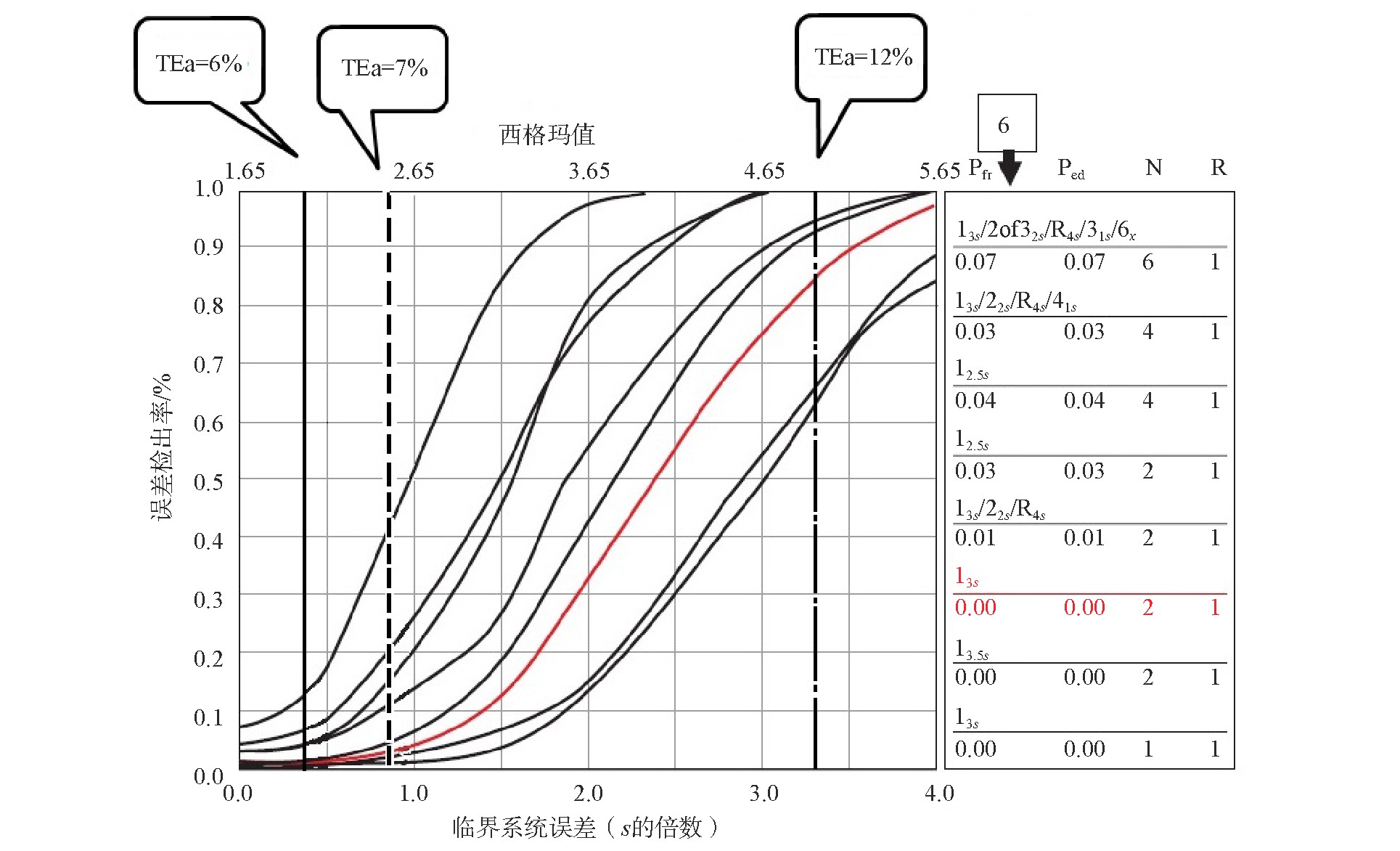
图2 基于3种不同质量要求的临界系统误差-西格玛质控图
3 讨论
糖尿病控制和并发症试验(the Diabetes Control and Complications Trial,DCCT)和英国前瞻性糖尿病研究(the United Kingdom Prospective Diabetes Study,UKPDS)均证实糖尿病并发症发病风险与糖尿病患者HbA1c水平有关[8-9]。目前,我国各级医疗机构检验科均开展了HbA1c检测,并以EQA的方式监测质量水平。国际临床化学和检验医学联合会推荐高效液相色谱串联电喷雾一级质谱法和高效液相色谱串联毛细管电泳法为HbA1c参考方法[10],但浙江省HbA1c项目EQA靶值仍为参加实验室公议值,评价方式为项目合格率。
虽然浙江省本次H b A1 c项目E Q A合格率>95%,但从西格玛水平看,结果并不乐观。西格玛度量值的计算结果因选择不同的TEa而不同,浙江省HbA1c项目的TEa较国际水平宽泛,计算所得加权西格玛平均值为4.95,但使用美国病理学家协会和我国国家卫生健康委临床检验中心的TEa时,加权西格玛平均值均<3。不同浓度水平及不同检测系统间的西格玛水平有较大差异。C组的组内CV和Bias最小,其西格玛平均值最高。选择TEa为6%时,仅C组的3个标本和B组的1个标本西格玛水平>3,其余均<3,甚至为负数,与章晓燕等[11]采用正确度验证计划的研究结果相近。以实现检验结果互认为目标,将相同检测系统甚至全省所有实验室看作一个整体,其西格玛水平为3时,代表其检测结果不符合率达6.7%,这个结果无法满足临床的要求。因此,在未实现HbA1c标准化和一致化的今天,建议在临床检验报告中注明检测系统及其参考范围。
目前,大部分实验室HbA1c检测的室内质控方案多按照美国临床实验室改进修正法规要求,即每天至少分析2个浓度水平的质控品。而根据本研究计算的西格玛水平,结合临界系统误差-西格玛质控图进行分析,结果显示,当选择美国病理学家协会标准时,即使选择最严格的质控规则和质控频率,也无法保证期望的误差检出率。如果将HbA1c应用于糖尿病的诊断,临床实验室需进一步改进HbA1c的检测性能,同时应加强室内质控,以提高误差检出率。
本研究采用的稳健算法来源于ISO 13528附录介绍的算法A,其客观性和可靠性已在本研究团队的前期研究中得到证实[7],结合六西格玛算法,不仅可评价单个实验室的检测性能,还可评价特定方法及特定方法间的性能特征,因此本研究建立的评价模型可推广至其他定量检测项目,尤其适用于无参考方法的检测项目。
虽然EQA未采用新鲜血液样本,质控品会存在一定的基质效应,影响西格玛度量的计算,但事实上,临床实验室通常会更谨慎地对待EQA结果,包括仪器的校准、保养和保证多次室内质控结果在控等措施,而且单独分组的实验室间的变异往往小于未分组的检测系统。此外,相关研究结果也表明,来源于HbA1c项目EQA参加者总体中位数的靶值与参考方法建立的靶值间差异并不明显[12]。因此,本研究计算的西格玛水平不一定较实际水平低,HbA1c项目实际的检测性能可能更不乐观。
综上所述,西格玛度量和稳健算法相结合的评价方式可更深入和客观地分析EQA结果。浙江省HbA1c检测的质量及可比性尚不理想,需进一步采取各项质量管理措施,以实现检验结果互认的目标,满足临床诊断糖尿病的需求。
参考文献
[1]中华医学会糖尿病学分会.中国血糖监测临床应用指南(2011年版)[J].中华糖尿病杂志,2011,3(1):13-21.
[2]中华医学会检验分会,卫生部临床检验中心,中华检验医学杂志编辑委员会.糖尿病诊断治疗中实验室检测项目的应用建议[J].中华检验医学杂志,2010,33(1):8-15.
[3]WEYKAMP C,JOHN W G,MOSCA A.A review of the challenge in measuring hemoglobin Alc[J].J Diabetes Sci Technol,2009,3(3):439-445.
[4]American Diabetes Association.Standards of medical care in diabetes-2010[J].Diabetes Care,2010,33(Suppl 1):S11-S61.
[5]王冬环,陈文祥.糖化血红蛋白诊断糖尿病的时代--糖化血红蛋白实验室检测指南解读[J].中国糖尿病杂志,2013,21(8):679-681.
[6]KANG F,WANG W,WANG Z.National survey on appropriateness of clinical biochemistry reporting in China[J].Clin Chem Lab Med,2015,53(11):1745-1751.
[7]康凤凤,王治国.一种新的室间质量评价靶值的建立与不确定度的稳健统计方法[J].检验医学,2013,28(9):854-855.
[8]Diabetes Control and Complications Trial Research Group,NATHAN D M,GENUTH S,et al.The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus[J].N Engl J Med,1993,329(14):977-986.
[9]UK Prospective Diabetes Study(UKPDS)Group.Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes(UKPDS33)[J].Lancet,1999,354(9178):602.
[10]JEPPSSON J O,KOBOLD U,BARR J,et al.Approved IFCC reference method for the measurement of Hb A1c in human blood[J].Clin Chem Lab Med,2002,40(1):78-89.
[11]章晓燕,王薇,赵海建,等.全国糖化血红蛋白正确度验证室间质评不同检测系统的结果分析[J].中华检验医学杂志,2015,38(11):742-745.
[12]居漪,吕元,唐立萍,等.上海地区各级医疗机构糖化血红蛋白正确度验证计划3年结果分析[J].检验医学,2015,30(11):1059-1069.




